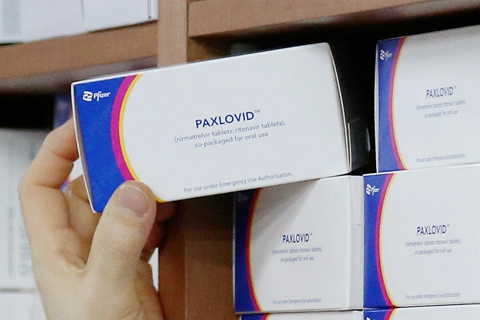
【财新网】5月23日晚,君实生物(01877.HK;688180.SH)公告称,由公司合作开发的新冠口服治疗药VV116在一项对比辉瑞新冠特效药PAXLOVID的三期注册临床研究中,达到方案预设的主要终点,药物的适应症为:用于轻中度新型冠状病毒肺炎的早期治疗。君实生物将于近期与监管部门沟通递交新药上市申请事宜。
此前,一项VV116在中国奥密克戎感染受试者中首个临床研究发布,相关论文手稿于5月17日发表在了医学期刊Emerging Microbes & Infections(EMI)平台。该研究是一项开放性、前瞻性队列研究,旨在评估VV116临床给药期间的安全性和病毒清除率(ORF1ab和N基因实时PCR Ct值>35)。
共有136名新冠肺炎确诊患者在3月8日至3月24日期间入组,其中VV116组60人,对照组76人。所有受试者均需要接受新冠肺炎标准治疗,VV116组受试者除接受标准治疗外,每12小时口服300mg VV116共持续5天(共10次)。在所有受试者中,有11.0%未接种新冠疫苗,0.7%接种一剂疫苗,45.6%完全接种两剂疫苗,42.6%接种了第三剂加强针。
研究数据显示,在首次核酸检测阳性5日内使用VV116的奥密克戎感染患者,其核酸转阴时间为8.56天,小于对照组的11.13天。有症状的患者中,在本研究的用药时间范围内(首次核酸阳性2-10天)给予VV116,均可以缩短患者的核酸转阴时间。在药物安全性上,使用了VV116的患者中,未观察到严重不良反应。
上述研究由国家传染病医学中心、上海市传染病与生物安全应急响应重点实验室、华山医院感染科张文宏团队与上海公共卫生临床中心范小红团队、临港实验室共同合作完成。需要指出的是,本次研究所有受试者均未发展为重症或危重症,仅初步评价了轻症患者中核酸转阴这单一指标。
VV116由君实生物、旺山旺水和中科院研发,是一种以RdRp聚合酶为靶点的小分子药物,在国产新冠口服药中研发进度居前。
此前君实生物公告称,VV116正处于国际多中心的III期临床研究阶段,包括针对中重度新冠肺炎患者评价VV116对比标准治疗的有效性和安全性的国际多中心、随机、双盲 III 期临床研究;针对轻中度患者评价VV116早期治疗的有效性、安全性和药代动力学的国际多中心、双盲、随机、安慰剂对照的II/III期临床研究。
本次揭盲的,VV116对比辉瑞新冠口服药Paxlovid(奈玛特韦片/利托那韦片)的多中心、单盲、随机、对照III期临床研究,旨在评估对比两者针对轻中度患者早期治疗的有效性和安全性。该研究已于今年4月完成首例患者入组及给药,实际入组822例患者。