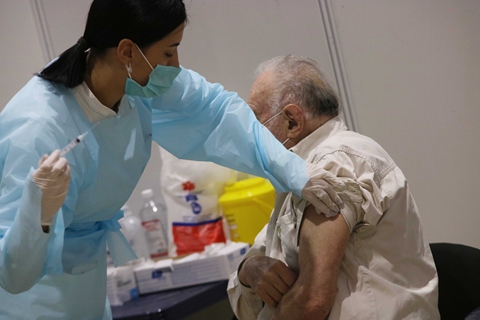
【财新网】(记者 王礼钧 实习记者 王卓青)当地时间2月4日,强生公司(NYSE:JNJ)的新冠疫苗已向美国食品药品监督管理局(FDA)提交了紧急使用授权(EUA)申请。
预计在这一申请得到批准后,强生疫苗将可以像辉瑞、莫德纳疫苗一样在美国推广使用。不过根据相关要求,需对试验参与者进行安全观察满两年后才能完成试验。强生公司方面表示,一旦得到批准,将立刻开始运输和分发疫苗。该公司也即将向欧洲药品管理局(EMA)提交有条件上市授权申请(cMAA)。
【财新网】(记者 王礼钧 实习记者 王卓青)当地时间2月4日,强生公司(NYSE:JNJ)的新冠疫苗已向美国食品药品监督管理局(FDA)提交了紧急使用授权(EUA)申请。
预计在这一申请得到批准后,强生疫苗将可以像辉瑞、莫德纳疫苗一样在美国推广使用。不过根据相关要求,需对试验参与者进行安全观察满两年后才能完成试验。强生公司方面表示,一旦得到批准,将立刻开始运输和分发疫苗。该公司也即将向欧洲药品管理局(EMA)提交有条件上市授权申请(cMAA)。
责任编辑:任波
版面编辑:许金玲
解药|美国一重组蛋白新冠疫苗保护率达89.3% 研发速度领先
2021年01月29日数字说|中国新冠疫苗已累计接种2277万剂次 各国接种进度几何?(更新中)
2021年01月27日财新网所刊载内容之知识产权为财新传媒及/或相关权利人专属所有或持有。未经许可,禁止进行转载、摘编、复制及建立镜像等任何使用。
如有意愿转载,请发邮件至hello@caixin.com,获得书面确认及授权后,方可转载。