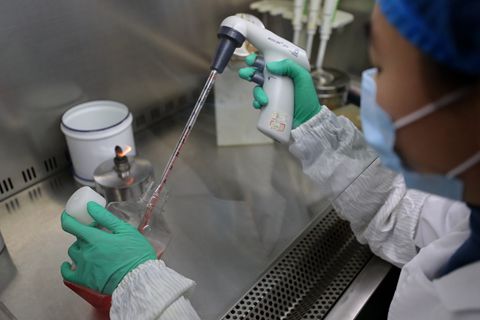
【财新网】国家药监局药审中心(CDE)日前发布《人源性干细胞及其衍生细胞治疗产品临床试验技术指导原则(试行)》(下称《原则》),对干细胞产品的临床试验做出规范。
干细胞有自我更新、多向分化潜能,是重要的再生医学产品,已在多种疾病上展示出巨大潜力,包括血液和淋巴系统疾病、强直性脊柱炎等免疫系统疾病、糖尿病等内分泌系统疾病、中风和阿尔茨海默等神经系统疾病以及肿瘤。clinicaltrials. Gov网站显示,截至目前共登记了9700多项干细胞产品相关的临床试验,其中约三分之一的研究处于一期临床或更早阶段。