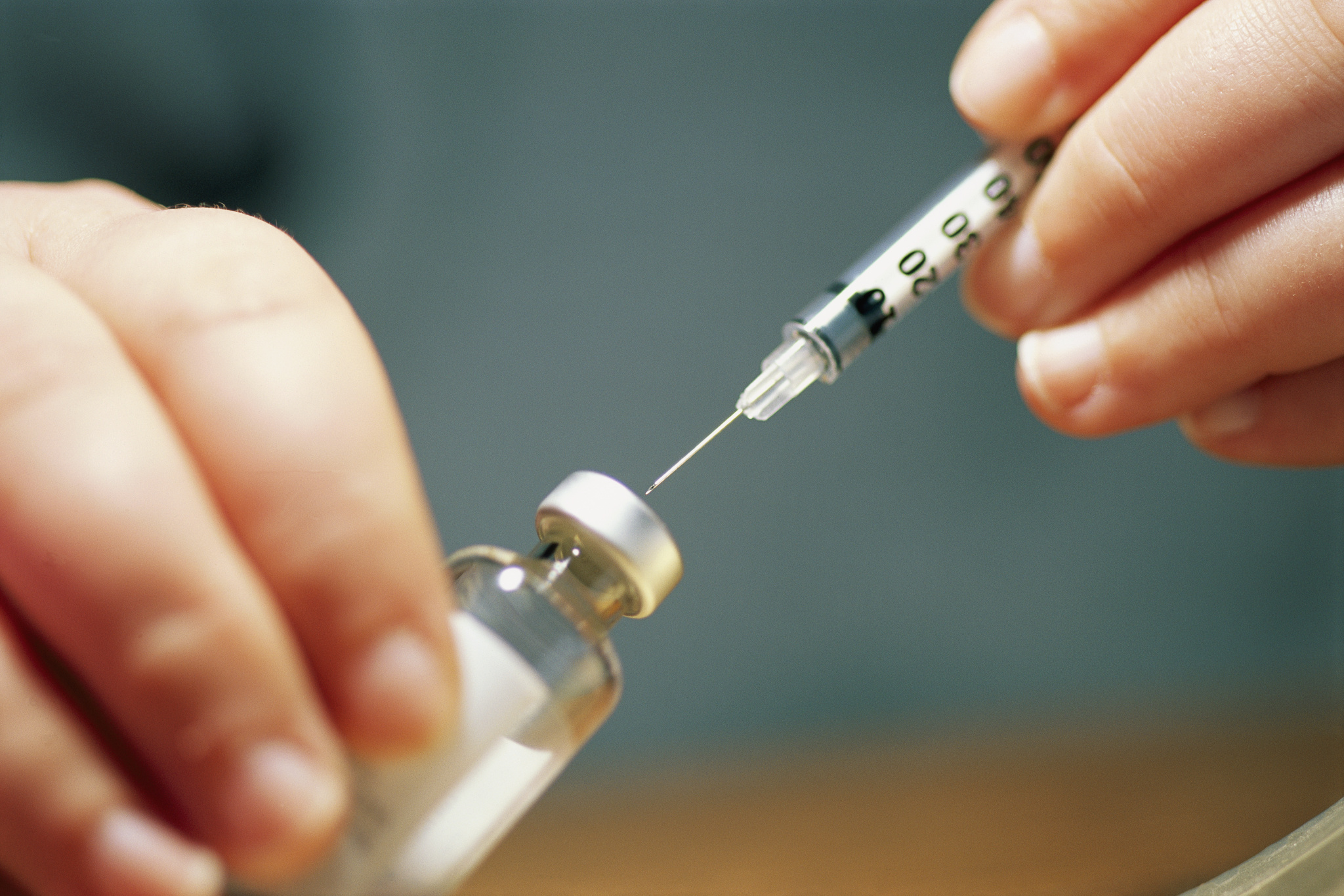
【财新网】(记者 梁振)注射剂一致性评价的进展或为相关企业带来利好。国家药品监督管理局药品审评中心10月15日(以下简称药审中心)第二次就注射剂一致性评价的技术要求和仿制药的申报资料要求发布征求意见稿。距离2017年12月第一次发布征求意见稿,新版的公布几乎时隔两年,这意味着期间注射剂一致性评价工作在官方层面陷入沉寂。
为指导仿制药一致性评价而推出的参比制剂目录中出现注射剂,这被外界视为官方要启动注射剂一致性评价的前兆。自2019年3月药审中心发布第21批参比制剂以来,注射剂品种开始集中出现。截至第24批,药审中心总计公布了628个注射剂参比制剂。